organizarea de celule chimice
Compoziția include aproximativ 70 de celule ale elementelor chimice ale DI sistemului periodic Mendeleev. În funcție de cât de multe elemente chimice incluse în substanțele care formează organism viu este acceptat să aloce mai multe grupuri ale acestora.
Un grup (aproximativ 98% în greutate din celule) formează patru elemente de lumină hidrogen, oxigen, carbon, azot. Acestea sunt numite macronutrienti. Acestea sunt componentele principale ale compușilor organici.
Un alt grup este format din elementele din interiorul celulei în cantități mai mici. Dintre acestea, sulf și fosfor, împreună cu macroelemente fac parte din compuși organici esențiali - acizi nucleici, proteine, grăsimi, carbohidrați, hormoni, potasiu, sodiu, magneziu, mangan, fier, clor efectua, de asemenea, funcții importante în celulă. Elementele conținute în celula în cantități foarte mici, se numesc micronutrienti.
Polaritatea moleculelor și capacitatea de a forma legături de hidrogen face apa un solvent bun pentru un număr foarte mare de substanțe anorganice și organice. Astfel de substanțe sunt numite hidrofile. În plus, apa asigură afluxul de substanțe în celulă și îndepărtarea deșeuri din acestea.
Apa are o conductivitate termică bună și capacitate termică mare, temperatură care să permită să rămână neschimbate la diferite temperaturi ambiante în mediul celular.
Cele mai multe celule substanță anorganică este sub formă de săruri - fie disociat în ioni, sau în stare solidă. Printre primele sunt cationilor mare importanță K, Na, Ca, iritabilitate care furnizează organismele vii. Din concentrația de sare din interiorul celulei depinde celulele memoria tampon. Tamponarea - celule capacitatea de a menține o reacție ușor alcalin al conținutului său, la un nivel constant în mediul în schimbare.
Compuși organici asupra medie, cu 20 - 30% din masa de celule. Acestea sunt polimeri biologici: proteine, acizi nucleici, glucide și lipide si unele molecule mici - hormoni, pigmenți, etc. ATP.
Proteine. Proteinele între substanțele organice ocupă primul loc, atât în număr și semnificație.
Proteinele sunt compuse din 20 de tipuri diferite de aminoacizi. Formula lor generală
unde R - structură radical diferit. În partea stângă a moleculei este gruparea amino din H2 N, care are proprietăți ale unei baze; carboxil COOH - - dreapta acidă, caracteristic tuturor acizilor organici. De aceea, aminoacizi - compus amfoter și proprietăți compatibilizare de acid și bază. Conectarea, moleculele de aminoacizi formează legături între acidul carbon și grupele de azot de bază. Astfel de legături sunt numite covalente, în acest caz - prin legături peptidice:
H2 N # 9472; HC # 9472; C + N # 9472; HC # 9472; COOH → H2 N # 9472; HC # 9472; C # 9472; N # 9472; HC # 9472; COOH + H2O
Compus format din 20 sau mai multe resturi de aminoacizi se numește o polipeptidă. Secvența de aminoacizi din catena polipeptidică numita structura primară a proteinei.
Cu toate acestea, molecula de proteină ca un lanț de aminoacizi, interconectate secvențial prin legături peptidice, nu este în măsură să îndeplinească funcții specifice. Acest lucru necesită o organizare structurală mai mare. Prin legarea de hidrogen între resturile carboxil și amină grupuri de diferite molecule de aminoacizi a proteinei ia forma unei spirale. Această structură secundară a proteinei. Dar, în cele mai multe cazuri, doar o moleculă care are o structură terțiară, poate efectua rolul biologic. Structura terțiară este formată prin interacțiunea dintre radicali, în special radicali aminoacizi cisteină care conțin sulf. Atomii de sulf din doi aminoacizi situate la o anumită distanță unul de altul sunt conectate, formând o așa numită disulfura sau S - S-bond. Găini helices polipeptidice în globulelor (bile) și se numește structura terțiară a proteinei (Figura 1).
Unele funcții ale corpului sunt realizate cu participarea proteinelor cu niveluri mai ridicate ale organizației - structura cuaternară. De exemplu, hemoglobina, insulina.
Pierderea unei molecule de proteină numită Denaturarea de organizare structurală (din latină denaturare -. Pentru a lipsi proprietățile naturale).
Renaturare - această proprietate de proteine restabili complet structura pierdut, în cazul în care nu schimba mediul a dus la distrugerea structurii primare.
Una dintre cele mai importante funcții de proteine intr-o celula - constructie. Proteinele uchuvstvuyut în formarea membranelor celulare in organite celulare si structurile extracelulare.
Extrem de important este funcția catalitică a proteinelor. Toți catalizatorii biologici - substanța fermenty- naturii proteinelor. Ei accelera reactiile chimice din celulă, în zeci și sute de mii de ori. Enzima catalizează doar o singură reacție, adică el uzkospetsifichen.
Funcția motorie a corpului este furnizat proteine contractile. Aceste proteine uchuvstvuyut în toate tipurile de mișcări, care sunt capabile de celule și organisme: pâlpâire cililor și bate flagella în cel mai simplu, contracția mușchilor la animale.
Funcția proteinelor de transport constă în unirea elementelor chimice (de exemplu, oxigen) sau substanțe biologic active (hormoni), și transferarea acestora la diferite țesuturi și organe ale corpului.
Atunci când organismul străin - proteinele sau microorganismele din celulele albe din sange - leucocite - format proteina speciala - anticorp. Ei se leagă și neutralizează substanțele străine organismului. Această funcție de protecție este exprimat proteine.
Proteinele sunt, de asemenea, una dintre sursele de energie în celulă, adică, îndeplini funcția de energie. La 1g plin clivaj proteină este alocat 17,6 kJ de energie.
Hidrati de carbon. Carbohidrații, zaharide sau - substanțe organice cu formula generală Cn (H2O) m.
Carbohidratii sunt împărțite în simple și complexe. hidrați de carbon sunt simple monozaharide. În funcție de numărul de atomi de carbon în moleculă sunt numite monozaharide triozele, tetroses, pentoze (riboză și dezoxiriboză), hexoze (glucoză, galactoză).
Carbohidratii complecsi, educați mulți monozaharide sunt numite polizaharide.
Carbohidrații două funcții principale: construcții (chitinei) și energie (amidon în plante și glicogen la animale - o rezervă de energie). Carbohidratii - sursa principală de energie în celulă. In timpul carbohidratii 1g oxidare 17,6 kJ de energie este eliberată.
Lipidele. Lipidele sau grăsimi, sunt compuși ai acizilor grași superiori moleculare și glicerol alcool trihidric. Grasimile nu se dizolvă în apă - acestea sunt hidrofobe. In celulele există întotdeauna alte substanțe grase cum ar fi - lipide.
Lipidele și lipide efectua construcții și funcția. acestea sunt o parte a membranelor celulare. Datorită săraci grăsime conductivitate termică capabilă să îndeplinească funcția unui izolator termic. Formarea unor lipide precede sinteza unor hormoni. Prin urmare, aceste substanțe este inerentă funcției de reglementare a proceselor metabolice.
Acizii nucleici. Nucleic (nucleu lat -. Nucleus) Acid - compus complex organ nical. Ele sunt compuse din carbon, hidrogen, acru, azot și fosfor.
Există două tipuri de acizi nucleici - ARN și ADN. Ele pot fi atât în nucleu și citoplasmă și organite sale.
ADN - acidul dezoxiribonucleic. Este un polimer biologic format din două lanțuri polinucleotidice cuplate TION unele cu altele. Monomerii - nucleotide care constituie kazh-suflare a ADN-ului, sunt compuși organici complecși. ADN-ul este format din patru baze azotate: derivații purinici - adenina (A) și guanină (G) și derivați pirimidinici - citozină (C) și timina (T), zahăr pentose pentahidrici - dezoxiriboză, și un rest de acid fosforic (Figura 2 ).
Nucleotidele fiecărei componente sunt unite prin legături covalente: un rest de dezoxiriboză nucleotidă cuplat cu nucleotidă acid fosforic ulterior. Cele două lanțuri sunt combinate într-o singură moleculă legături de hidrogen care apar între bazele azotate care alcătuiesc nucleotide care formează diferite circuite. bază spațială azotată con-figurația este diferit și numărul de astfel de con-legături între diferite baze de azot inegal. Dupa-Corolarului, ele pot fi conectate numai în perechi viespi azotate Considerații adenina (A), un lanț de sex și de nucleotide este întotdeauna conectat, dar două legături de hidrogen cu timină (T), un alt lanț și guanina (G) - trei legături de hidrogen cu baza azotată citozina -niem (C) opusă polinucleotide tse-rinichi. O astfel de capacitate de compus selectiv nucleo-tidov, în care se formează o pereche de A-T și G-C, numita complementaritate (vezi fig. 15). Dacă o secvență de baze cunoscută a unui lanț (de exemplu, TJ T-T-A-T), apoi prin principiul complementarității (complementaritate) vor fi cunoscute și secvența de bază opusă (A-G-T-A-D) .
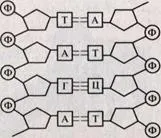
Figura 2. Reprezentarea grafică a moleculei de ADN. nucleotidele complementare compus diferite lanțuri.
lanțuri de nucleotide formează pravozakruchennye vrac spin-Rali de 10 baze în fiecare bobină. Secvență Cps-neniya o catenă nucleotidă opusă a Dru-goy, adică lanț care cuprinde o moleculă de ADN raznonaprav-mai puține la număr sau antiparalelă: internucleotidelor secvență legături din cele două circuite, în direcția în direcții opuse: 5 „-3“ și 3 „-5“. grupe de zahar fosfat de nucleotide sunt camping afară, și azotate bază TION - interior. Lanț răsucite una în raport cu cealaltă și față de axa comună pentru a forma o spirală dublă th. Această structură a moleculei mo-susținută, în principal, prin legături de hidrogen (Fig. 3).
Pentru prima structură secundară ADN, a stabilit mai întâi american Bio-log fizician Dzh.Uotson engleză și Crick.

Fig.3 structura ADN-ului dublu helix: A - model de plan, o linie groasă reprezintă coloana vertebrală-zahăr fosfat; B - model de volum
Când ADN care unește cu proteine specifice (histone) grad helix molecule crește - tam-tam-pocaieste superspiralDNK a cărui grosime crește semnificativ, iar lungimea este redusă (figura 4). Unitatea de compactare servește moleculă ADN nucleozomului, care se bazeaza pe 8 molecule de histone, 2 din fiecare tip (H2A, H2B, și H4 NS). Suprafețele acestor molecule proteice transporta sarcini pozitive și abordarea-formează un schelet în jurul căruia răsucire poate fi molecula negativ-negativ-taxat ADN. Fiecare nucleozomilor WMOs-dit de la 146 la 200 de perechi nukleoti-rânduri. Histone cincilea tip - N1 - se leagă la situsurile de ADN, legarea de o nucleozomului th alta. Acest ADN se numește liniar sau Comm-țional - linker. Nucleo
soma aranjate de-a lungul ADN-ului la o anumită distanță, inegală în funcție de tipul de celulă - la 20 la 50 nm. Aceasta formează o structură similară cu mărgele, în care fiecare perlă - nucleozomului.
Fig. 4 Schema de ADN super-helix.

Nucleosomi și ADN linker la rândul său, ambalate în fibrile, care formează bucle pe cromozomul. Niveluri mai ridicate helix poate reduce semnificativ lungimea moleculei de ADN. Este suficient să spunem că moleculele de lungime mo-ADN-ul total cuprinzând cromozomi umani este de 1,74 m, acestea sunt situate în celulele având un diametru de 5 microni -7. Această moleculă, cu atenție „ambalate“ proteine pot fi on-au fost observate la microscop în timpul diviziunii celulare precum și pătată -hromosomy vițel alungit.
ARN - acid ribonucleic. ARN precum și ADN-ul este un polimer al cărui monomeri sunt aproape NUS-leotidy nucleotidelor ADN. baze azotate trei nucleotide aceeași ca cea inclusă în ADN (adenina, gua-ning, citozină), al patrulea motiv - uracil (U) este prezentă doar în molecula de ARN (în loc de timină). Nucleotidele Otley nucleotide ARN-ADN nu sunt similare cu structura și carbohidrat constituent: acestea includ alt pentoză - riboză (în loc desault-ksiribozy). RNKnukleotidy lanț legat prin formarea de legături covalente între ribozei de nucleo-ghid și un acid fosforic reziduuri celălalt.
Conform distinge structura dublu catenar și un ARN monocatenar. ARN păzitori genetice dublu spiralate de informații TION unui număr de virusuri, de exemplu, îndeplini funcția lor de cromozomi. ARNm cu lanț unic transporta informații despre secvența de aminoacizi din proteine (adică, din structura proteinelor) a cromozomilor din locația lor de sinteză și de a participa la sinteza proteinelor.
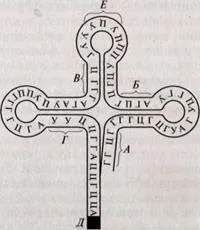
Fig.5 Structura circuitului de ARNt: A, B, C, T - porțiuni de picior complementaritate, un mol de compus din cadrul kuls-ARN; D - secțiunea (situs activ) cu un compus amino; E - secțiune (centru activ) compus Comp cu o moleculă elementară și ARN (anticodon)
Există mai multe tipuri de ARN monocatenar. Numele lor se datorează pentru a îndeplini funcția sau locația în celulă. Cele mai multe dintre ARN citoplasmatic (80 - 90%) Compoziția doresc să stabilească ARN up-ribozomal (ARNr) informațiile conținute în ribozomi. Mole Kula ARNr relativ mică și este format din 3 - 5 mii de nucleotide .. Un alt tip de ARN - informații (ARNm), transferul la informația ribozomi schaya secvență aminokis-Lot in proteine care trebuie sintetizat. Dimensiunea porțiunii ADN dependentă de ARN de lungime la care sunt sintetizate. Și molecule de ARN poate fi compus din 300 - 30 000 de nucleotide. Tran-Sportna ARN (tRNA) includ 76 - 85 nucleotide (Fig.) Și îndeplini mai multe funcții. Ele asigură aminoacidul în loc sinteza proteinelor și realizate precis orientarea aminoacizilor (pe baza complementarității) la ribozom. ARNt are două site-uri active, dintre care unul este conectat la aminoacid definit divizat și celălalt format din trei rânduri nukleoti servește pentru conectarea la o moleculă de ARNm complementar. Această zonă este numită anticodon.