Cercetarea procesului de politropic - studopediya
Scopul acestei lucrări este definiția practică a indicelui politropic când gazul din vas în mediu.
Un rezumat al teoriei
Numele acestui proces este combinația a două cuvinte grecești „poli“ - și o mulțime de „TROPOS“ - un fel, și anume politropice.
Raportul dintre parametrii termici (P, V, T) într-un proces de politropică se caracterizează prin următoarea relație:
PV n = const sau n; (11)
TV n-1 = const sau n-1; (12)
TP (1-n) | n = const sau (1-n) / n; (13)
unde P - presiunea absolută, H2 / m; V - volumul specific, m3 / kg; T - temperatura absolută, K; n - politropic exponent n în procesul termodinamic particular poate fi orice valoare în intervalul de la - ∞ la + ∞, rămânând constantă); CV, CP și C specific (masa) capacitatea calorică a procesului, respectiv izocoră, izobare și politropic, J / (kg x K).
Căldura specifică într-un proces de politropică depinde de indicele politropic și poate fi determinată de formula,
h = (C-CP) / (C-CV), care este transformat obține
unde R - raportul căldurilor specifice,
# 956; CP # 956; CV - specific (kilomolnaya) calorice a gazului în timpul izobară și respectiv izocoră, J / (K x kmol).
Valoarea numerică a indicelui R adiabatice pentru gaze diferite atomice pot fi determinate prin formula (15) utilizând Tabelul 2 de date.
După cum se poate observa din tabelul. 2, diferența # 956; CP - # 956; CV pentru gaze diferite atomice are aceeași valoare care este egală cu 8314 J / (K x kmol). Această diferență este notată cu # 956; R este numită constanta universală a gazelor, iar expresia
În cazul în care R = # 956; R / # 956; - gaz constantă J / (kg x K).
căldură Kilomolnaya la P = const și V = const și valorile indicelui adiabatice pentru diferite gaze de Atomicitate
Figura 3. Dependența căldura specifică a indicelui politropic
dependența grafică a capacității calorice specifice a indicelui politropic este prezentat în Fig. 3, din care rezultă că capacitatea calorică C într-un proces politropic, dacă k> n> 1 este o valoare negativă. Prin urmare, în procesele care au loc la o valoare dată a indicelui politropic, dg și dT au diferite semne algebrice. Cu alte cuvinte, în cazul în care un fluid de lucru în procesul de la k> n> 1 este alimentat de căldură, scade sale de temperatură și când retragerea căldurii - este crescută. (După exemplul Parsed confirmă această poziție).
Locație politropic în pV și Ts - coordonate pentru diferite valori ale indicelui politropic n, este prezentată în Fig. 4, care arată că un gaz politropică schimbare de stare de proces în ceea ce privește anumite procese termodinamice (izocoră, izobare, izoterme și adiabatice) este o umbrelă.
Într-adevăr, în cazul în ecuația (11) pentru a lua:
n = 0, obținem ecuația izobata (p = const);
n = 1, obținem ecuația izotermei (pV = const).
n = k. Obținem ecuația adiabatic (pV R = const);
n = ± ∞. isochore obținem ecuația (V = const).
Capacitatea termică specifică a proceselor termodinamice private pot fi determinate din Fig. 1 sau cu formula (13); când n = 0 (proces izobară) specific Cp capacitate termică;
>> n = 1 (proces izotermic) >> C t = ± ∞;
>> n = k (un proces adiabatic) >> Cs = ± ∞;
>> n = ± ∞ (proces izocoră) >> Cv = ± ∞.
Utilizarea uneia dintre diagramele (figura 2) poate fi definit ca un anumit proces în timpul expansiunii sau comprimare a gazului și cunoscut exponent politropic variază presiunea gazului, volumul său, temperatura, energia internă și entropie, și de asemenea, efectuate sau scoase din căldura de proces a gazului. De exemplu, se cunoaște din practică, că comprimarea aerului (gaz diatomic) în cilindrul compresor, care este echipat cu o manta de apă de răcire, realizată la un politropică exponent n ≈1,35.
În acest caz, compresia aerului politrope (valoarea k = 1,41 pentru care) este situat între izotermă 1-4 „si 1-5 adiabatic“ și k> n> 1 (vezi. Fig. 2), care poate fi determinată și logic .
Teoretic există două cazuri extreme de proces de comprimare a gazelor în compresor:
1. Căldura eliberată de gaz de compresie este complet retrasă în mediul extern și temperatura gazului comprimat rămâne neschimbat - comprimarea izotermă.
(Compresia izotermică este posibilă în cazul în care procesul este infinit perioadă lungă de timp, în care diferența de temperatură dintre gazele arse și mediul extern dT = 0).
2. Compresia gazului produs în peretele cilindrului, care sunt
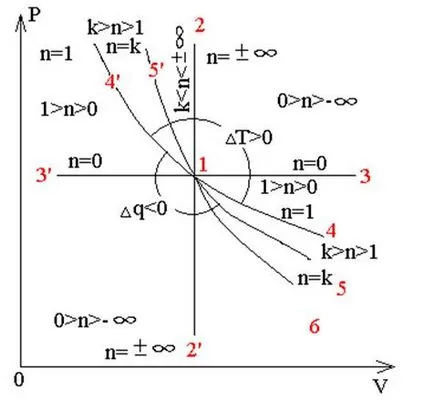
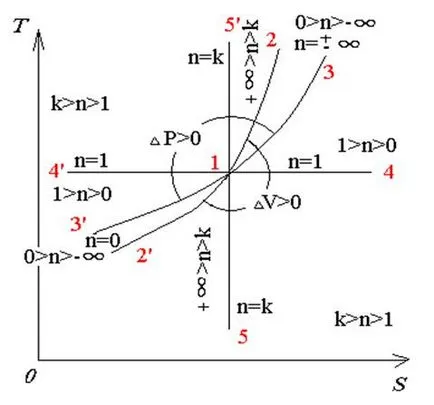
Fig. 4. Domenii de posibile procese Polytropic (a) și (b) diagramele TS PY
izolator absolut, iar căldura degajată de gazul de compresie este complet consumată pentru încălzirea gazului comprimat (aziabatnogo caz de compresiune).
În compresorul real, gazul este comprimat într-o cantitate finită (relativ mic) de timp; peretele cilindrului compresor din material conductor termic (apă răcită din exterior). Prin urmare, în compresor reale, Chota și căldură sunt schimbate între gazul szhatymnagrevshimsya și apă de răcire, ca urmare a proceselor rapide de compresie ea până la sfârșitul timpului pentru a obține prin intermediul. Acest lucru se schimba nu numai parametrii termici T, p și V. dar gazul adică entropia S. există proces de compresie politropic, care este situat între izoterma și adiabatic.
Utilizarea diagramelor (Figura 2). definesc modul în care schimbările în acest proces ne interesează valoarea:
1) volumul scade de gaz - (# 916; V <0);
2) de lucru de comprimare a gazelor - negativ (L <<->>), Care rezultă din formula # 916; L = p # 916; V;
3) temperatura crește de gaz comprimat - (# 916; T> 0);
4) energia internă a gazului (# 916; U> 0) crește ca # 916; U = c # 916; T;
5) o presiune a gazului, comprimat în compresor este crescut (# 916; F> 0);
6) entropia gazului scade (# 916; S <0), поскольку его сжатие ведется с отводом теплоты (Δq <0 или q <<->>), Și entropia și căldura legată de dS = dq / T;
7) valoarea indicelui politropic «n» este la k> n> 1.
muncă specifică, J / kg, expansiunea gazului într-un proces de politropică poate fi determinată prin una dintre următoarele formule:
J căldură specifică / kg, un proces politropic
și modificarea entropiei gazului J / (kg x K),
Pentru a determina indicele politropic n în orice proces real, există moduri destul de simple. Astfel, în cazul în care procesul de eliminare diagramă indicatoare (.. A se vedea figura 2), apoi pentru a determina n valoare medie, de exemplu în procedeul 1-6, utilizând ecuația (10) pentru cele două puncte la care valoarea V p și parametrii cunoscuți:
După ce a luat logaritmului au
Ordinea de execuție a lucrărilor de laborator
Determinarea indicelui n politropic pentru aer în timpul expansiunii sale se realizează pe o setare de laborator într-o astfel de secvență (Figura 5.):
Cu ventilatorul în cilindrul 1, cu un robinet deschis 2 se injectează aer.
2. După crearea presiunii în exces în interiorul recipientului PM1 = 1000 N / m2 robinet 2 este închis, iar ventilatorul este deconectat de la duza de evacuare.
3. Deoarece temperatura aerului de supraalimentare, ca rezultat al compresiei ar fi ceva mai mare decât temperatura mediului ambiant, apoi pentru a elimina această diferență face parte din expunerea (cinci minute). Când acest lucru are loc procesul de izocoră - scăderea temperaturii în interiorul containerului, având un volum constant. Pentru procesul de izocoră, raportul parametrilor termic p și T este exprimată prin ecuația
Fig. 5. Diagrama laboratorului de configurare de lucru 2:
1 - un recipient din sticlă; 2 - stopcock propkovy; 3 - manometru lichid în formă
Pe alinierea temporală a aerului comprimat în temperatura cilindrului la temperatura ambiantă promisiunea final măsurarea presiunii în interiorul vasului este determinată prin intermediul U - în formă de manometru 3. Presiunea excesivă a aerului comprimat, astfel, oarecum redus de la PM1 la P3.
4. Deschideți supapa 2. Ca urmare a presiunii în cilindrul de expansiune a gazului scade la cea atmosferică. La această temperatură, situată în scăderile de tancuri. Reducerea temperaturii gazului în timpul expansiunii sale se datorează faptului că activitatea de expansiune se realizează în detrimentul energiei interne, adică l reducă. Energia internă a gazului este legată de relația temperatura U = CVT.
5. Robinetul 2 este închis. Apoi produc expunere (cinci minute), pentru egalizarea temperaturii aerului din cilindrul de temperatura mediului extern. Când acest lucru se întâmplă în procesul de cilindru izoterma (cu aport de căldură din mediul înconjurător la aerul din rezervor).
Pe alinierea temporală a temperaturii gazului din cilindru și aerul exterior la capătul presiunii de măsurare proces din interiorul cilindrului definit prin intermediul U - manometru în formă.
P3 Presiunea absolută în container devine mai mare decât cantitatea de atmosferic Rb PM3.
exponent Polytropic pentru gazul de test bazat pe următoarele considerații sunt calculate într-un proces politropic.
Ca urmare a expansiunii adiabatică a raportului de gaz a parametrilor termici T și P este exprimată prin ecuația (12).
Ca urmare a expansiunii adiabatice a unui gaz de proces trebuie izocoră proces de încălzire, pentru care, în conformitate cu (20), raportul dintre parametrii T și F au exprimat prin ecuația
Cu toate acestea, condițiile experimentale, T1 = T3 = Tamb, prin urmare, au
Prolagorifmiruem ultima expresie:
n = ----------, (25)
unde P1 = P m1 + Rb; RB - presiunea barometrică la momentul experienței; PM1 - ecartament (manometru) presiunea gazului din rezervor, înainte de expansiune; P3 = Rb + P m3; PM3 - ecartament (manometru) presiunea gazului din recipient, după expansiunea și apoi urmată de încălzire izocoră.
Ca regia de către șeful valorii P1. Rb și R3 în formula (25) este substituit în una din următoarele unități: N / m 2; mm coloană de apă (Kg / m 2); mm Hg si altele.
În raportul următoarele informații ar trebui să fie incluse pe munca de laborator:
1.) Scopul și ordinea de performanță;
2.) Schema de configurare de laborator;
3.) Rezultatele datelor experimentale, rezumate în tabelul 5;
4.) Schimbările în procesul de imagine starea gazului în experimentul p v Ts - coordonatele și compararea acestuia cu izocoră, izobară, izotermă și adiabatică.
1. Procedura lucrării de laborator.
2. termodinamic (politropic și private) procese observate în natură și tehnologie.
3. Raportul dintre parametrii termici într-un proces politropic.
4. Capacitatea de căldură și procesele termodinamice politropice private.
procese 6. fotografie Polytropic în fotovoltaică și Ts - coordonează și compararea acestora cu procesele termodinamice private.
7. Determinarea diagramei politropic indicele proces de afișare.
/ 4 /, p. 25-55; / 5 / s. 57-58.