92 Curs 1
1.1. Concepte de bază și definiții
Sistemul termodinamic este o colecție de corpuri într-o regiune a spațiului trebuie să fie studiul termodinamic. În cazul extrem, sistemul este format dintr-un singur corp.
Sistemul este separat de suprafața reală sau imaginară a mediului.
Materia - este tot ceea ce ne înconjoară.
Energia - este măsura mișcării materiei. Unitatea de energie este joule (J).
Între organismele și transferul de energie de mediu are loc sub formă de căldură și de muncă.
Căldura - este o formă de transfer de energie prin schimb de căldură. Cantitatea de căldură în termodinamică notată Q. Unitatea de căldură (precum și unitatea de alimentare) este Joule (J).
Căldura specifică se numește căldură, menționată la 1 kg de greutate corporală și este notat cu q. Dimensiunea sa J / kg.
Iov - o formă de transfer de energie prin intermediul interacțiunii mecanice dintre corpurile. Volumul de muncă în termodinamică notat simbolul L. Lucrarea unitate este, de asemenea, joule (J).
muncă specific este de lucru menționat la 1 kg de greutate corporală. Acesta este notat cu simbolul l. este, de asemenea, dimensiunea J / kg.
Schimbul de căldură - este o formă de transfer de energie, care nu sunt asociate cu activitatea și interacțiunea directă dintre microparticule (conducție sau convecție) sau cu propagarea undelor electromagnetice (radiația termică).
Organul de lucru este numit corpul, prin acțiunea care are loc la interconversia de căldură și de muncă.
În cazul motoarelor de aeronave pentru fluidul de lucru este aerul sau un amestec de aer cu produsele de ardere.
Sistemul Energoizolirovannoytermodinamicheskoy este un sistem care nu face schimb de energie cu mediul înconjurător.
Un izolat termic (adiabatică) sistem termodinamic este un sistem care comunică cu mediul de lucru numai.
Chemat un sistem omogen, compoziția chimică și proprietățile fizice în toate părțile sale componente identice sau schimba în mod continuu, fără salturi. În caz contrar, sistemul este eterogen.
Sistemele pot fi deschise sau închise. Sistem închis - un sistem în care substanța nu se schimbă (Figura 1.1a.). Pereții și pistonul
Acestea sunt limita reală a sistemului.
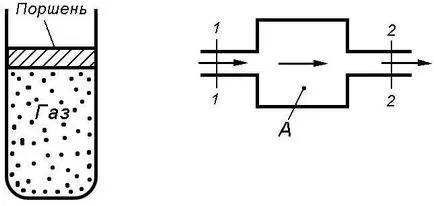
Fig. 1.1. Exemple de sisteme termodinamice
a) - sistem termodinamic deschis
b) - un sistem termodinamic închis
Sistem deschis - un sistem în care compoziția substanței se modifică (Figura 1.1b.). Aici, secțiunea 1-1 și 2-2 - părțile imaginare ale suprafeței, adică, granițele imaginare ale unui sistem termodinamic. În cazul motoarelor cu turbină cu gaz, dispozitivul A poate fi un compresor, combustor, turbine, etc.
Equilibrium starea sistemului se numește starea sistemului, în cazul în care este, după izolarea de mediul nu se schimbă starea. Apoi, la fiecare punct de parametri termodinamici (temperatură, presiune, densitate etc.) nu variază în timp și nu există nici un transfer de energie de la o parte la alta.