substanțe complexe duritatea apei

substanțe complexe
Substanțele complexe - substanțe chimice este format prin îmbinarea mai multor substanțe simple. Într-o economie din ce în ce mai complexe substanțe care le folosim și într-o măsură mult mai mică - o substanță simplă.
Prin noi substanțe folosite includ sare complexă (punct chimic c de vedere) oxizi. bază sau alcaline, acizi. precum și mulți compuși organici cum ar fi alcooli, parafine, aldehide etc.
norma zilnică de apă
Apa - un solvent puternic. Crezi că, la ce temperatura apei cântărește mai mult?
Cea mai mare densitate a apei este fixată la 4 ° C, deasupra și sub această temperatură, densitatea scade treptat. În consecință, și cântărește mai apă la 4 ° C
Apă distilată până la gust diferit de la robinet. Acest lucru se datorează faptului că în apă dizolvată zeci obișnuite de săruri diferite, - o sare de calciu (prezență împiedică formarea acestor săruri în soluție de săpun de rufe), magneziu (de obicei, dă apă amară), precum și săruri de fier, metale alcaline și multe alte materiale.
Apă îmbogățită cu ioni metalici utili pentru corp (dar nu de la robinet!). De exemplu, potasiu și magneziu - pentru mușchii cardiaci, calciu si fier - pentru coagularea sângelui, sodiu - pentru formarea de săruri minerale având o reacție alcalină și capabilă să degradeze materie organică.
Toată lumea știe că organismul uman este de 81% apă și, desigur, întotdeauna nevoie de completarea acesteia. Prin urmare, rata de apă care primesc suzhestvuet corpului uman, în funcție de greutatea persoanei:
duritatea apei
duritatea apei permanentă nu poate fi îndepărtat prin fierbere. O astfel de apă conține săruri - sulfați, cloruri, nitrați, calciu, magneziu. Dar puteți obține încă scăpa de duritatea apei constantă: folosiți lapte de var (hidroxid de calciu - Ca (OH) 2) sau un suc.
Una dintre cele mai eficiente mijloace pentru a elimina duritatea apei constantă este utilizarea de ortofosfat de sodiu (Na3 PO4). Prin reacția cu apă sărată, care dau duritatea apei, precipitarea:
Când apa fierbe pe ustensilele pereți rigizi formate scum - calciu și săruri de magneziu. Ele sunt conductoare slabe de caldura. În cazul în care scara a fost format mult, ustensile de perete se poate supraîncălzi.
Atunci când spălați în apă săpun greu consumă considerabil mai mult. Acest lucru se datorează formării de complexe de substanțe insolubile în apă - calciu și magneziu stearați (Ca (C17 H35 C00) 2 și Mg (C17 H35 COO) 2)
În apă și legumele sunt fierte greu mai deoarece carbohidrații conținute în legume pentru a forma săruri de calciu și magneziu compuși complecși insolubili.
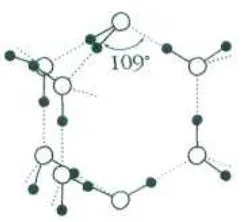
Apă și gheață. De ce apa este mai grea decât gheață?!
Fragmentele (H2 O) 8 și depozitate în apă lichidă. In interiorul acestor agregate pierde o parte din moleculele de H2O, astfel încât densitatea apei este mai mare decât densitatea de gheață (900 kg / m 3)
Despre jet de apă potabilă:
Toți știu că neutralizarea apei curgătoare produse folosind clor, sau mai degrabă o soluție care conține clor. Micro-organisme într-un astfel de mediu nu poate supraviețui și să moară. Dar deteriorează astfel calitatea apei, deoarece clorul - foarte puternic oxidant reacționează cu impuritățile dizolvate în ea și formează compusul organoclorine dăunătoare pentru sănătate. Unele dintre substanțele cele mai toxice și nocive - dioxine. Aceste substanțe - sunt reale otrava! Acestea afectează organismele umane încalcă funcționarea corespunzătoare a acestora. Nu întotdeauna și filtrele pot face față cu o overabundance de clor dizolvat.
Dintre toate apa de pe planeta noastră, doar 1% este potabilă. În ciuda faptului că există o largă varietate de diferite filtre de curățare, chiar și cel mai bun filtru (care cuprinde straturi de mediu schimbător de ioni, cărbune activat) nu este capabil să îndepărteze toate substanțele toxice din apă. obține apă curată poate fi un filtru de înlocuire regulat (cartuș), prin urmare, este necesar să se ia în considerare sursa de la care este luat apa și cum se curăță (de exemplu, într-o zonele deosebit de poluate, filtrul trebuie schimbat mai des, deoarece se va deteriora).
apă foarte curat și sănătos este obținut din surse naturale, care este pre-procesat, în continuare purificat și îmbuteliată în sticle de sticlă!
Zapada se formează atunci când picăturile de apă microscopice în nori de particule de praf sunt atrase și sunt înghețate. cristale de gheață care, astfel, nu par să depășească 0,1 mm în diametru, în primul rând, se încadrează în jos și cresc datorită condensării umezelii din aer. Într-o asemenea mișcare, formată sub formă cristalină hexagonală. Prin structura moleculelor de apă între vârfurile dimensiunilor cristaline pot forma unghiuri de doar 60 și 120 de grade. Principala Apa cristalină are în plan orizontal, formează un hexagon regulat. Pe partea de sus a acestei noi cristale hexagonale depuse pe ele - noi si forma astfel diferite forme de stele - fulgi de zăpadă.

La o temperatură suficient de ridicată în mod repetat, cristalele se topesc și se cristalizează din nou. Acest lucru încalcă dreptul forma de fulgi de zăpadă, și formează un soi mixt. Cristalizarea toate cele șase unghiuri fulgi de zăpadă are loc simultan în condiții practic identice și, prin urmare, unghiurile de formă fulgii obținut, de asemenea, la fel.
Din punctul de vedere al cristalografie forma cea mai naturală este fulgi de zăpadă „hexagonală“ simetrie. În același timp, în natură este fulgi de zăpadă triunghiulare pe scară largă rasprostrastraneny. Motivele pentru această diferență de până acum rămân necunoscute.
Pentru a forma fulgi de zăpadă triunghiulare necesită o temperatură de 2 grade sub zero.
Un nou studiu realizat de fizicienii americani cuantifica impactul unor factori asupra creșterii de fulgi de zăpadă. După cum considera fizica, sunt 2 factori majori: dinamica difuzie a moleculelor de apă în aer și comportamentul dinamic al acestor molecule la suprafața cristalului. Ei au putut stabili că acești parametri sunt determinați direct de fluxul de aer, care acoperă un fulg de nea. Supoziții teoretice oamenii de știință testate folosind un „mașini de zăpadă“ - camere, care pot fi utilizate pentru a controla creșterea de fulgi de zăpadă. Ca urmare, sa stabilit că fulgii triunghiulare sunt cele mai rezistente, adică schimbarea în fluxul de aer nu se schimba forma de fulgi de zăpadă. Acest lucru, potrivit oamenilor de știință, explică răspândirea de fulgi de zăpadă triunghiulare.
Mai recent, oamenii de știință din Marea Britanie a reușit să obțină „pentagon“ fulg de zăpadă. Ei au pus un strat subțire de particule de gheață pe suprafața de cupru. Acest strat de molecule de apă sunt situate în nodurile pentagonul.
Promovarea site-ul cu garanția Kazan O
Alege-și cumpăra mixer www.santehnika.kh.ua/smesiteli/ la un preț accesibil în magazinul online.
Comutarea în engleză
Substanțe complexe. duritatea apei