Q 6 № clor proprietăți chimice caracterizează
Q № 6 CaracterizaŃi proprietăți chimice de clor. Asigurați ecuația reacțiilor chimice, arătând:
a) reacția litiu și clor;
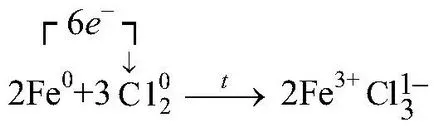
b) arderea pulberii de fier în clorul;
c) arderea hidrogenului în clor;
g) reacția clorului cu apă. Pune jos oxidarea semnelor chimice. Explicați că oxidat și ceea ce este redusă în aceste reacții.
1) Clorul reacționează cu substanțe simple care acționează ca oxidant:
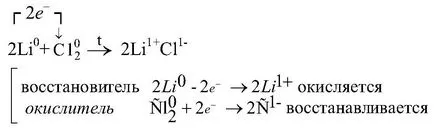
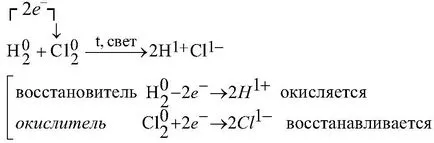
2) reacționează cu apa de clor; în această reacție, clorul este agentul de oxidare și agentul reducător simultan:
3) clor reacționează cu alcalii; în aceste reacții este, de asemenea, un clor oxidant și reducând în același timp:
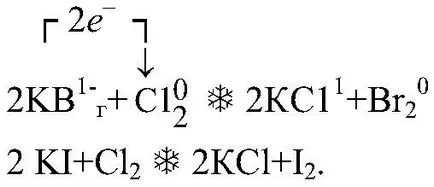
4) substituția bromului sare clor și iod; în aceste reacții este oxidant clor: