proprietăți ale aminoacizilor
Amino Acid (AA) - molecule organice care constau din grupări amino primare (-NH2), o grupă de acid carboxilic (-COOH) și un radical R organic (sau catene laterale), care este unic pentru fiecare AK
amino acizi funcția în organism
Exemple de proprietăți biologice ale AK. Desi au fost observate în natură mai mult de 200 de curent alternativ diferit doar aproximativ o zecime din ele sunt incluse în proteine, altele efectuează alte funcții biologice:
- Acestea sunt elementele constitutive ale proteinelor și peptidelor
- Precursorii multor molecule biologic importante derivate AK. De exemplu, tirozina este precursorul compusului tiroxina hormonului și pigment de piele melanina, tirozină și precursorul DOPA (dihidroxi-fenilalanină). Această transmisie puls neurotransmițător în sistemul nervos. Triptofanul este un precursor al vitaminei B3 - acid nicotinic
- Surse de sulf - AK sulf.
- AK sunt implicate in multe cai metabolice, cum ar fi gluconeogeneză - sinteza glucozei in organism, sinteza acizilor grași și alții.
În funcție de poziția grupării amino la gruparea carboxil a AK poate fi alfa, α-, beta, β- și gamma, γ.
Alpha - grupare amino atașată la carbonul adiacent la gruparea carboxil:
Beta - grupa amino situat la al 2-lea carbon din gruparea carboxil
Gamma - grupă amino la 3a ugleroe din gruparea carboxil
Structura proteinelor merge numai alfa-AK
Proprietățile generale ale alfa-AK proteină
1 - Activitatea optică - aminoacizi proprietăți
Toate AK pentru glicină isklyuchekniem, prezintă activitate optică, deoarece conțin cel puțin un atom de carbon asimetric (atom chiral).
Ce este un atom de carbon asimetric? Acest atom de carbon la care sunt atașate patru substituent chimic diferit. De ce glicină nu prezintă activitate optică? radicale doar trei substituenți diferiți Săi, adică, alfa-carbon nu este asimetric.
Ceea ce înseamnă că un optic activ? Aceasta înseamnă că AK în soluția poate fi prezentă în cei doi izomeri. izomer dextrogir (+), care are capacitatea de a roti planul luminii drept polyarizatsovannogo. izomer levogir (-), care are capacitatea de a roti planul luminii polarizate spre stânga. Ambii izomeri se pot roti planul de polarizare a luminii pentru un aceeași sumă, dar în direcția opusă.
2 - proprietăți acido-bazic
Toate AK conțin cel puțin două grupări ionizate - alfa-amino și grupa alfa-carboxil. Unele dintre ele conțin în lanțul său lateral mai multe grupări acide sau bazice, care sunt responsabile pentru comportamentul acid-baza AK
Ca urmare, capacitatea lor de a ionizare poate scrie echilibrul acestei reacții:
R-COOH<-------> R-C00 - + H +
Deoarece aceste reacții sunt reversibile, acest lucru înseamnă că ei pot acționa ca acizi (reacție directă) sau ca baze (reacția inversă), ceea ce explică proprietățile amfoteri ale aminoacizilor.
Ion amfoter - AK proprietate

Polaritatea totală a proprietății aminoacizi
La pH fiziologic AK prezent ca amfioni taxa iony.Polozhitelny poarta alfa-amino și negativ carboxilic. Astfel, se creează două taxa protivovolozhnyh la ambele capete ale moleculei moleculei AK are proprietăți polare.
Prezența punctului izoelectric (IEP) - Proprietatea amingokislot
PH-ul la care sarcina electrică netă este nulă aminoacizi, și, prin urmare, nu se poate deplasa într-un câmp electric este numit pI.
Capacitatea de a absorbi ultraviolete - aminoacizi aromatici proprietate
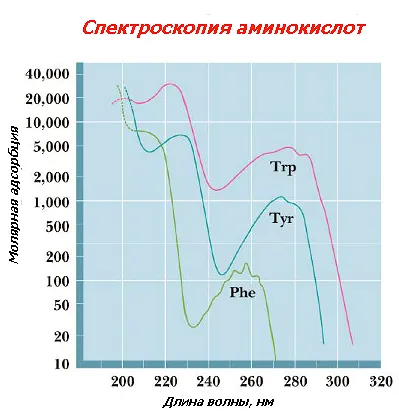
Fenilalanina, histidină, triptofan și tirozină absorb la 280nm. Fig. otorazheny un coeficient de extincție molară (ε) de AA. Partea vizibilă a spectrului de aminoacizi nu absorb, prin urmare, ele sunt incolore.
AK poate fi prezent în doi izomeri variante: izomer L și D-
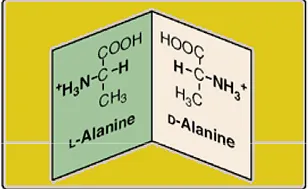
Toți aminoacizii din proteinele din configurația L, L-aminokicloty.
Proprietățile fizice ale aminoacizilor
Aminoacizii sunt, în principal, solubil în apă, datorită polaritatea lor și prezența grupărilor încărcate. Ele sunt solubile în polari și nu se dizolvă în solvenți nepolari.
AK au o temperatură de topire ridicată, care reflectă prezența unor legături puternice care susțin zăbrele lor de cristal.
Proprietățile generale ale AK este comună tuturor AA și în multe cazuri determinate de alfa-amino și gruparea alfa-carboxil. AK posedă proprietăți specifice, care sunt dictate de catena laterală unică.