Lab № 1 familiarizare cu elementele de bază ale calculului schimbătoarelor de căldură în procedeul din exemplul
3 Informații teoretice
3.1 Cele mai importante proprietăți ale soluției prin evaporare
La o soluție de proprietăți relevante pentru procesul de evaporare includ depresia temperaturii, capacitatea calorică și căldura de dizolvare.
În același temperatura T, presiunea vaporilor peste solventul pur Ra este mai mare decât presiunea de vapori de deasupra soluției Pg. și, în consecință, pentru una și aceeași presiune Manpower temperatura de fierbere a solventului mai mică decât punctul de fierbere al soluției.
T -const

Manpower-Const

Diferența dintre soluție și temperatura de fierbere a solventului numit depresie
unde Tr-ra - temperatura de fierbere a soluției;
Tr-la - punctul de fierbere al solventului;
Pentru a determina ΔD / există mai multe formule:
- soluții concentrate de substanțe nedissotsiiruyuschih
unde Rμ = 8,31 - gaz universal constant J / mol · K;
Bp - punctul de fierbere al solventului, K;
Deoarece - concentrație, moli / moli de solvent solut;
r - căldura molară de evaporarea solventului, J / mol.
- pentru soluți disociat:
unde i - raportul dintre numărul total de particule, obținut prin disociere, cu numărul inițial de particule de solut.
depresia Temperatura poate fi determinată empiric prin ecuația
unde - constant determinată empiric.
De obicei, ΔD / necalculat, și a găsit tabelele.
3.1.2 depresie hidrostatică
depresia hidrostatica caracterizează crește punctul de fierbere al soluției cu o presiune tot mai mare a coloanei de fluid hidrostatic. depresia hidrostatica se manifestă numai în dispozitive cu o soluție la fierbere în tuburile din camera de încălzire cu abur. În acest caz, temperatura de fierbere a soluției ia un punct de fierbere în mijlocul țevilor de încălzire.
unde
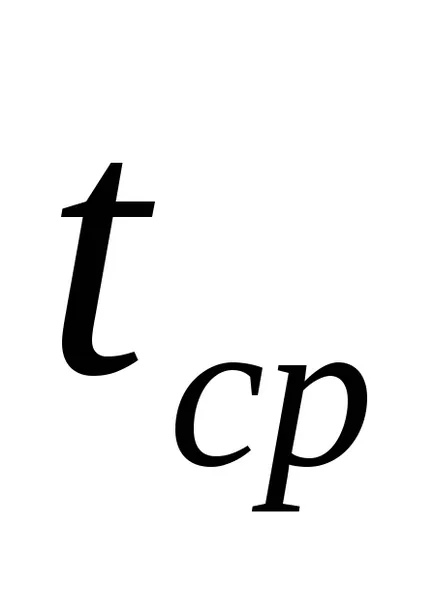
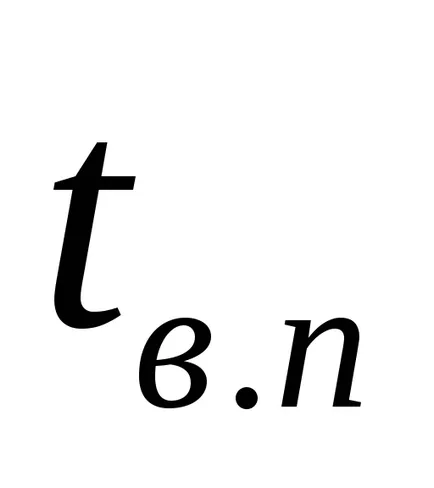
Presiunea din partea de mijloc a țevilor de încălzire este determinată de expresia
unde H - înălțimea fierberea tuburilor, m;
ρpzh - densitatea amestecului vapori-lichid în aparat, kg / m3.