Determinarea însărcinarea moleculei de peptidă
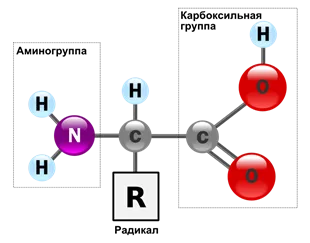
Peptidele - compuși organici din aminoacizi. unite prin legături peptidice.
Aminoacizii pentru cea mai mare parte, astfel de molecule sunt:

Legătura peptidică este formată după cum urmează:
R (radical) pot fi diferite. Radicali aminoacizi proteinogenici care trebuie învățate sunt prezentate în tabelul de mai jos:

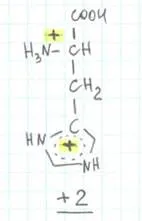
Să considerăm o posibile opțiuni câteva acidității mediului:

2. Mediul de mai puțin acid la neutru, să presupunem că un pH de aproximativ 5 (adică cantitatea de H + este redus). Protonii nu mai sunt suficiente pentru o grupare carboxil (primul lucru din proton este întotdeauna pierde-l), dar celelalte două dispoziții sunt încă protonate.

3. Un mediu neutru și cazul său special - punctul izoelectric (aceasta corespunde histidină la pH 7,6). Punctul izoelectric al taxei nete de aminoacizi este zero. Protonii sunt numai în gruparea amino.
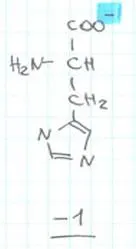
Prin urmare, pentru a determina încărcătura peptidei este necesară pentru a determina încărcătura aminoacidului care intră în compoziția sa, în funcție de aciditatea mediului.
Ce taxa va avea o peptidă constând din 3 molecule de histidină într-un mediu foarte acid? Pentru a face acest lucru, să conta cât de multe poziții ar putea fi protonat (atașați un proton).
1. Două dintre cele 3 grupe amino și două dintre grupările 3-carboxil sunt implicate în formarea legăturii peptidice - nu poate fi protonate.
2. Disponibilă rămâne o grupare amino (N-terminal al peptidei) și o grupare carboxil (C-terminal). De asemenea, 3 reziduuri imidazol.
Gruparea amino N-terminal ne-ar da un pic plus, trei reziduuri de imidazol 3 mai semnul plus, și o grupare carboxil - zero.
Total. taxa peptidei His-His-His într-un mediu acid foarte este 4+
Și ce va fi responsabil de peptida Gli-Gli-Gli în mediul acid? Se repetă procedura.
1. Două dintre cele 3 grupe amino și două dintre grupările 3-carboxil sunt implicate în formarea legăturii peptidice - nu poate fi protonate.
2. Disponibilă rămâne o grupare amino (N-terminal al peptidei) și o grupare carboxil (C-terminal). radical Glicina - N. protonate nu se poate.
Gruparea amino N-terminal ne-ar da un pic plus, radical trei ne dau trei zerouri, iar carboxi alt zero.
Total. taxa peptidei Gly-Gly-Gly într-un mediu acid este egal cu 1 +.
În acest mod (pe examinarea constituenților) și taxa de peptidă determinată.