Compoziția vaporilor - studopediya
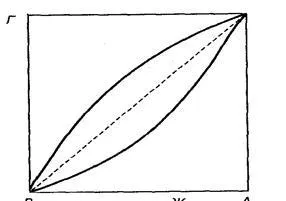
Fig. Compoziția de echilibru lichid și vapori
Diagonala unui pătrat corespunde cazului când formulările de vapori și de soluție sunt egale. Abaterile de voința diagonală mare, cu atât mai mare diferența de presiunea de vapori a componentelor în formă pură.
6. Diagrame compoziție - soluții punct de fierbere
În acest caz, este necesar să se compare soluțiile care nu sunt la aceeași temperatură și aceeași presiune. Una dintre cele două lichide fiind comparate, care are o presiune de vapori mare, la aceeași temperatură, are un punct de fierbere scăzut. Menținerea stării primite vom fi notate cu componenta B, având un punct de fierbere mai scăzut.
În diagramele, reprezentând dependența temperaturii de fierbere a compoziției, luate în mod tipic pentru a construi două curbe, dintre care unul conectează aceste temperaturi cu compoziția fazei lichide, iar celălalt - cu compoziția pereche, așa cum se vede în figură. Aici, curba inferioară se referă la formulări lichide (curba lichidă) și superioară - la compoziții perechi (pereche curba).
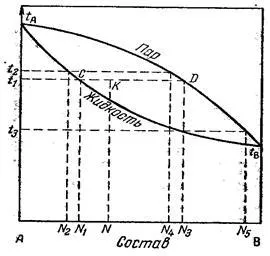
Fig. Figura compoziție - punctul de fierbere al amestecurilor binare.
La un t1 temperatură (la o presiune dată) va fierbe compoziția de mortar x1. echilibru a vaporilor cu soluția, are o compoziție x3.
Poziția punctului care indică compoziția oricărui sistem eterogen, determinat de cantitățile relative ale fiecăreia dintre faze. În cazul în care cantitatea de vapori și lichid sunt, respectiv moli Nn și NZH, raportul dintre segmente și CK KD tăiat cu punct de sistem eterogen K va fi egal cu CK / KD = Nn / NZH.
regulă maneta. Punctul corespunzătoare compoziției eterogene a sistemului binar este situat pe punctele liniei de îmbinare care reprezintă fazele coexistente. Când acest punct intercepta pe o linie care este invers proporțională cu cantitatea fiecăreia dintre faze.
cutie diagrama situată sub curba lichidă reprezintă starea de soluții de compoziție diferită, la temperaturi sub temperatura de fierbere (câmp fluid). câmp diagrama de mai sus curba de vapori reprezintă starea de vapori de compoziție diferită, la temperaturi peste temperatura de condensare în (cutia de abur) fluid. Zona dintre curbele corespunde sistemelor eterogene lichid și vapori, constând dintr-un echilibru între soluția lichidă și abur.
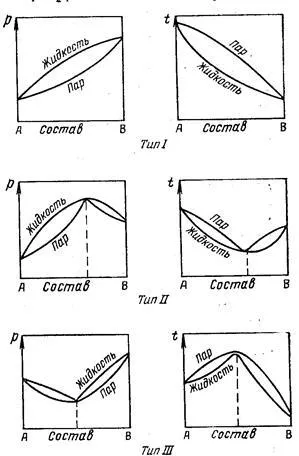
Pentru sistemele cu deviere semnificativă de la linia de presiune legea lui Raoult în funcție de compoziția vaporilor au un maxim (cu o abatere pozitivă) sau minim (pentru abatere negativă).
Sistemele cu un maxim la curbele de presiune a vaporilor, curbele au un minim de temperatura de fierbere, și invers.
Soluțiile care corespund punctelor de maximă sau minimă se numesc soluție azeotrop sau inseparabil de fierbere. Ele fierbe integral formate la temperatură constantă și nu pot fi separate prin distilare.
Fig. compoziția Diagramele - presiunea vaporilor și compoziția - punctul de fierbere pentru diferite tipuri de sisteme